기술&제품
[배터리101] 눈에는 안 보이는 배터리 속 세상
2024.06.14
|
명사 뒤에 붙는 숫자 ‘101[wʌ́nouwʌ́n]’은 기초 과정, 입문, 기본이라는 뜻입니다. '배터리101'은 배터리가 궁금한 모든 이들을 위한 입문서로, 배터리의 역사부터 기초 원리, 구동 원리 등 기술적인 부분과 IT, 전기자동차, ESS 등 산업적인 부분, 그리고 차세대 기술과 삼성SDI가 열어갈 미래의 모습이 담겨있습니다. 배터리가 만들어갈 더 나은 세상은 우리의 상상보다 무한할 것이기에, ‘배터리101’을 통해 그 세상 속에서 삼성SDI의 역할을 되새기면 좋겠습니다. |
배터리는 4대 요소로 구성된다
1차전지가 처음 나왔을 때, 사람들은 원통형 배터리 안에 쌓여 있던 전기가 선을 타고 흘러 나온다고 생각했습니다. 그래서 다 써버린 배터리를 빈 깡통으로 간주했고, 이를 뜯어보거나 못으로 뚫어보는 등 대수롭지 않게 취급했습니다. 이는 배터리 안에 무엇이 들어있는지 몰랐기에 가능했던 위험한 행동이었습니다.
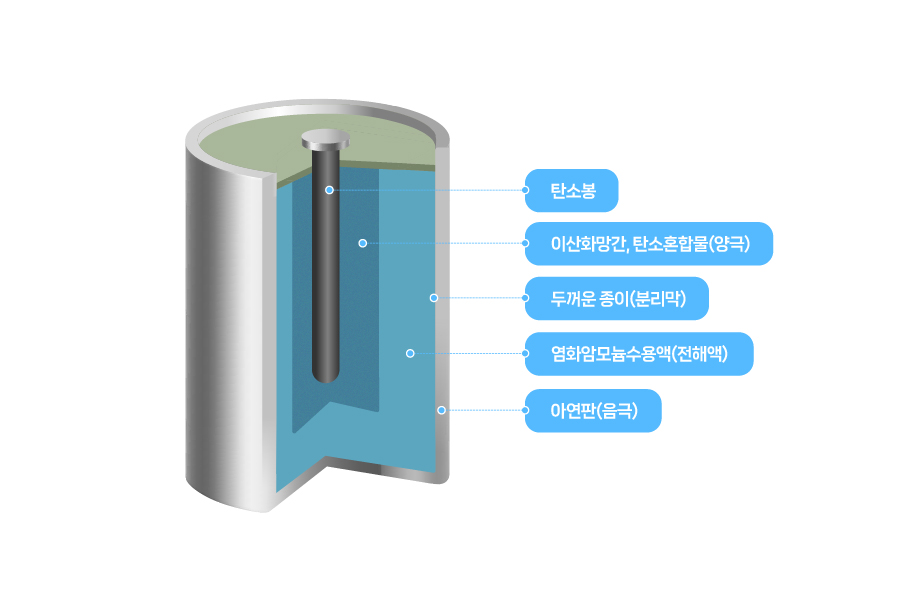
[망간전지의 구조]
1차전지와 2차전지는 모두 음극, 양극, 분리막, 전해질의 4대 구성요소로 이루어집니다. 전해질과 같이 액체 형태로 흡수되어 바로 확인이 어려운 경우도 있지만, 눈으로도 쉽게 구분할 수 있습니다. 2차전지 중 리튬이온 배터리를 중심으로 4대 구성요소의 특성을 간략히 살펴보겠습니다.
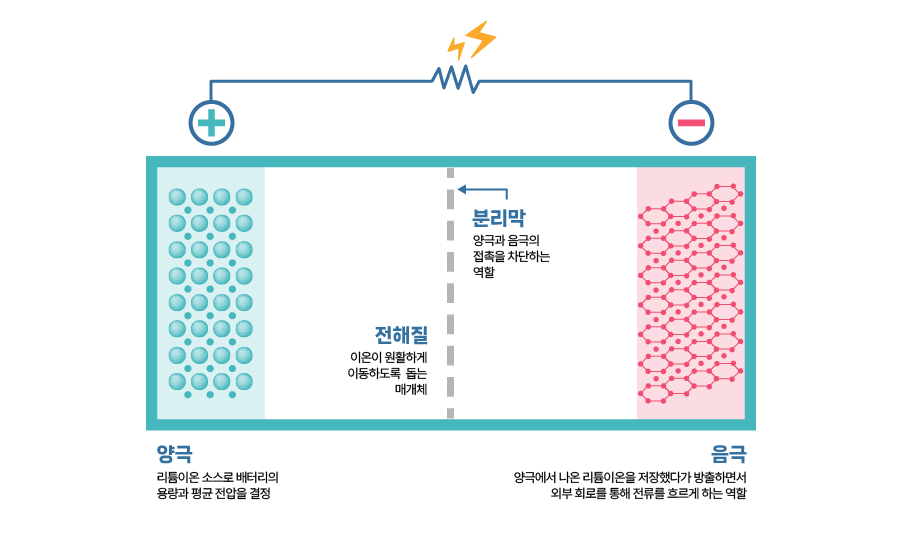
[리튬이온 배터리의 4대 구성요소]
먼저 양극은 배터리의 성능과 스펙을 결정짓는 요소입니다. 배터리의 특성을 이야기할 때 가장 먼저 떠올리는 것이 용량과 출력인데, 양극에서 이 부분을 담당합니다. 배터리의 전압은 양극의 전위차에 의해 결정되므로 양극 구조에 따른 전위값이 전압에 큰 영향을 줍니다. 이에 따라 업계에서는 양극의 성능 향상을 위해 양극 활물질을 개선하는 데 주력하고 있습니다. 여기서 활물질(active material)이란 에너지가 들어 있는 물질을 말합니다. 리튬이온 배터리의 경우, 양극의 금속은 알루미늄(기재)을 사용하지만 활물질은 리튬금속산화물을 사용합니다.
알루미늄은 전류(전자)를 수집하는 역할을 하고, 이렇게 수집된 전류는 탭(전지의 극과 닿는 부분)을 통해 흐릅니다. 충전 시에는 전자를 내주는 산화 반응이 일어나고, 방전 시에는 전자를 받는 환원 반응이 일어나는데 이때 산화와 환원 반응에 참여하는 것은 알루미늄이 아니라 리튬금속산화물입니다. 다시 말해, 어떠한 리튬금속산화물을 쓰느냐에 따라 배터리의 용량과 전압이 결정되는 것입니다.
음극의 역할은 양극에서 내보낸 전자와 리튬이온을 받아 보관했다가 방전 시 이를 방출하는 것입니다. 전자는 외부 회로로 이동해 전류를 흐르게 하고 리튬이온은 전해질을 통해 양극으로 이동합니다. 이때 음극에 있는 전자가 방전 시 전류를 흐르게 하는 원천이 되어, 전류의 공급원이 됩니다.
음극 활물질은 양극 활물질과 마찬가지로 배터리 용량에 큰 영향을 미칩니다. 음극에서 전자를 수집하는 역할을 담당하는 것은 구리(기재)입니다. 다양한 소재의 양극 활물질에 비해 음극 활물질은 주로 흑연을 사용합니다. 흑연의 경우 전자와 이온을 받았다가 내보내는 과정에서 물리적인 팽창과 수축을 반복하는데, 이는 배터리 수명에 영향을 미칩니다.
분리막은 양극과 음극의 물리적인 접촉을 막습니다. 리튬이온 배터리의 양극과 음극이 닿게 되면 단락(short)이 발생해 화재로 이어질 수 있기 때문입니다. 특히 리튬 소재는 높은 반응성을 가지고 있어 더욱 위험합니다. 분리막은 이러한 상황을 막아주어 배터리의 안전성을 높이는 데 중요한 역할을 담당합니다. 따라서 높은 절연성과 열 안전성이 요구되며, 일정 이상의 온도에서는 자동으로 이온의 이동을 막는 기능을 갖춰야 합니다.
전해질은 이온은 통과시키고 전자는 출입하지 못하게 하여 외부 도선으로 이동시킵니다. 따라서 이온전도도가 높은 물질이어야 하고, 안전을 위해 전기화학적 안전성과 발화점이 높아야 합니다. 높은 이온전도도를 위해 주로 액체가 사용되며 최근에는 폴리머나 세라믹을 같이 사용해 액체 전해질의 점도를 조절하는 경우도 있습니다. 이 경우 물처럼 흐르지 않게 되므로 안전성이 보강되지만 공정이 추가됨에 따라 비용이 상승합니다.
리튬이온과 전자가 이동하며 전기를 만든다
2차전지는 반복해서 충방전이 가능한 만큼 경제적이고 친환경적입니다. 전기자동차의 경우 내연기관 자동차 대비 탄소 배출이 월등히 적습니다. 이처럼 충전이 가능한 배터리의 발명과 고용량, 고출력을 향한 발전은 우리의 삶에 매우 큰 의의를 지니고 있습니다. 다음 그림은 충전과 방전 시 이온의 흐름을 나타낸 것입니다.
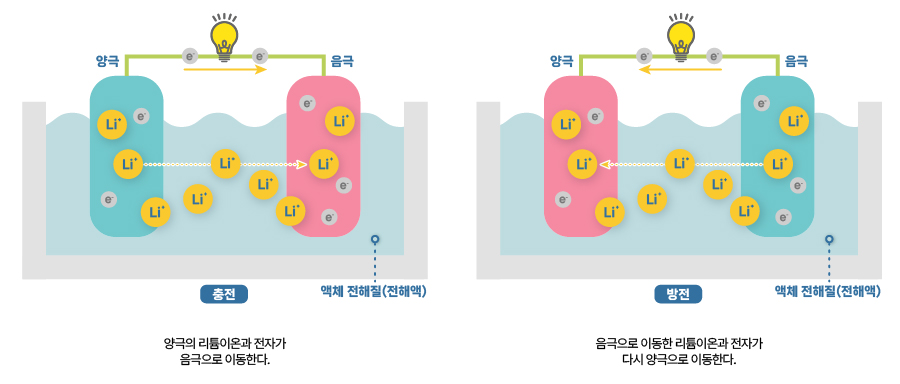
[리튬이온 배터리의 충전과 방전]
그림의 노란색 동그라미는 리튬이온, 회색 동그라미는 전자를 나타냅니다. 2차전지를 충전하면 양극에서는 산화 반응이 일어나고 음극에서는 환원 반응이 일어납니다. 양극에 쌓여 있던 전자는 도선을 타고 음극으로 이동하고 리튬이온은 전해질을 통해 음극으로 이동하며, 방전 시에는 이런 과정이 반대로 이루어집니다.
일반적으로 금속 원자는 전자가 빠져나오지 않아 양극도 음극도 아닌 상태입니다. 이 금속 원자가 화학전지에 장착되면, 양극 소재와 음극 소재의 이온화 경향의 차이로 인해 전자가 빠져나오고 양이온이 분리되어 나옵니다. 빠져나온 전자는 도선을 타고, 양이온은 전해질을 타고 같은 방향으로 이동합니다. 이 과정에서 전기가 발생해 전자기기가 작동됩니다. 이때 양극에서 벌어지는 일이 환원 반응, 음극에서 벌어지는 일이 산화 반응입니다.
대부분의 사람들은 배터리를 교체하지 않아도 스마트폰을 2년 이상 사용합니다. 실제로 정상적인 환경에서 스마트폰 배터리 용량이 80% 수준으로 유지되는 기간은 2~3년 정도입니다. 80% 아래로 성능이 떨어져도 큰 불편함을 느끼지 못하는 경우가 많기 때문에, 체감상 사용 기간은 오히려 더 긴 편입니다. 이는 더 강한 배터리를 위해 진행되고 있는 4대 구성 요소에 대한 연구 개발 덕분입니다.
